Zielgerichtete Therapien in der gynäkologischen Onkologie
Autorin:
Dr. Irina Tsibulak
Universitätsklinik für Gynäkologie und Geburtshilfe
Medizinische Universität Innsbruck
E-Mail: irina.tsibulak@i-med.ac.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Rezente Fortschritte der molekularen Krebsforschung führen zur Etablierung personalisierter und auf der Tumorbiologie basierender Therapien. In der gynäkologischen Onkologie sind Hemmer der Angioneogenese, Poly(ADP-Ribose)-Polymerasen(PARP)- sowie Immuncheckpoint-Inhibitoren bereits seit Jahren in Verwendung. In den letzten Jahren haben jedoch weitere zielgerichtete Therapien neue Perspektiven eröffnet. Hier spielt vor allem eine neue Substanzklasse der Antikörper-Wirkstoff-Konjugate eine wichtige Rolle.
PARP-Inhibitoren beim Ovarialkarzinom
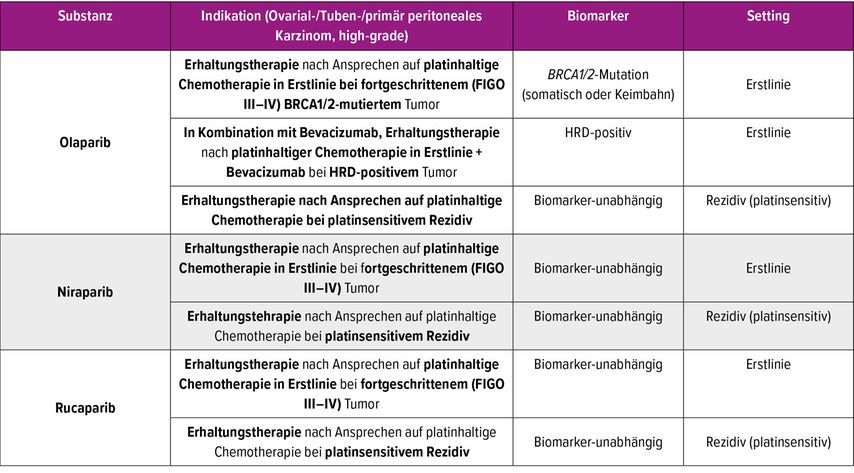
Ein paradigmatischer Durchbruch in der Behandlung des epithelialen Ovarialkarzinoms gelang durch den Einsatz von PARP-Inhibitoren. Diese Substanzen nutzen das Konzept der „synthetischen Letalität“: Tumorzellen mit Defekten in der homologen Rekombinationsreparatur (HRD), insbesondere BRCA1/2-Mutationen, sind besonders anfällig für die Blockade der PARP-vermittelten DNA-Reparatur. Aktuell sind PARP-Inhibitoren für die Erhaltungstherapie sowohl nach der Erstlinienbehandlung als auch im Rezidivsetting zugelassen. Die genauen Indikationen sind in der Tabelle 1 zusammengefasst.
Tab. 1: In der Europäischen Union für die Behandlung des High-Grade-Ovarialkarzinoms zugelassene PARP-Inhibitoren
PARP-Inhibitoren haben ein charakteristisches Nebenwirkungsprofil, das v.a. hämatologische und gastrointestinale Toxizitäten umfasst. Häufig treten Anämie, Thrombozytopenie und Neutropenie auf, weshalb regelmäßige Blutbildkontrollen (initial monatlich, später nach klinischer Einschätzung) obligat sind. Bei klinisch relevanter Myelosuppression werden eine Dosisreduktion, Unterbrechung oder ggf. Therapieabbruch empfohlen. Zu den nicht-hämatologischen Nebenwirkungen gehören Übelkeit, Erbrechen, Fatigue und Appetitlosigkeit, die meist durch symptomatische Maßnahmen (Antiemetika, Ernährungsempfehlungen, Pausen) beherrschbar sind. Seltener, aber klinisch bedeutsamsind sekundäre maligne Erkrankungen wie myelodysplastisches Syndrom (MDS) oder akute myeloische Leukämie (AML), weshalb bei persistierenden hämatologischen Auffälligkeiten eine hämatologische Abklärung erfolgen sollte.
Angiogenese-Hemmer
Bevacizumab ist ein monoklonaler Antikörper, der gezielt gegen den Vascular Endothelial Growth Factor A (VEGF-A) – den zentralen Botenstoff in der Angioneogenese – gerichtet ist. Bevacizumab ist sowohl bei fortgeschrittenem oder rezidiviertem Ovarial- als auch bei persistierendem, rezidivierendem oder metastasiertem Zervixkarzinom etabliert. Durch Hemmung der Tumorangiogenese werden das Tumormikromilieu verändert und die Wirksamkeit der Chemotherapie verstärkt.
Die Nebenwirkungen von Bevacizumab ergeben sich aus seiner antiangiogenen Wirkung. Häufig treten arterielle Hypertonie und Proteinurie auf; daher sind regelmäßige Blutdruck- und Urinkontrollen wichtig, bei Bedarf erfolgt eine antihypertensive Therapie oder eine Unterbrechung der Behandlung.
Blutungen (v.a. Epistaxis, seltener schwerwiegende gastrointestinale oder pulmonale Blutungen) sowie thromboembolische Ereignisse können auftreten und erfordern ein sorgfältiges Abwägen bei Risikopatient:innen. Eine klinisch bedeutsame, wenn auch seltene Komplikation sind gastrointestinale Perforationen, die zum sofortigen Absetzen zwingen. Ebenfalls relevant sind Wundheilungsstörungen, weshalb Bevacizumab mindestens 28 Tage vor und nach größeren chirurgischen Eingriffen pausiert werden sollte. Das Management der Nebenwirkungen basiert auf präventiver Überwachung (Blutdruck, Urinstatus, klinische Symptome), rechtzeitiger Pausierung sowie symptomatischer Therapie.
Immuncheckpoint-Inhibitoren
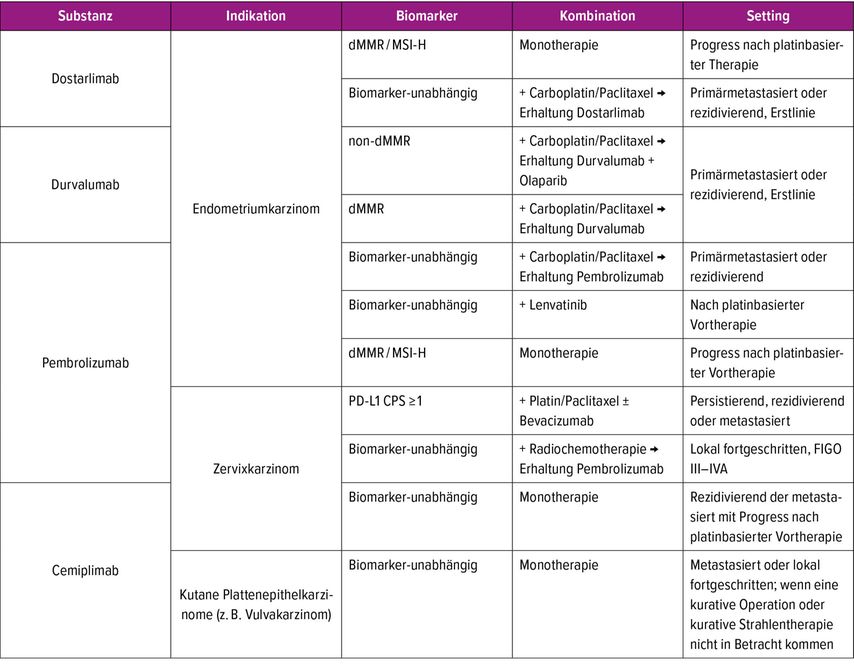
In der gynäkologischen Onkologie haben Immuncheckpoint-Inhibitoren, insbesondere Antikörper gegen PD-1 (z.B. Pembrolizumab, Dostarlimab, Nivolumab) oder PD-L1 (z.B. Atezolizumab), zunehmend an Bedeutung gewonnen. Ihr Einsatz basiert auf der Blockade von Immuncheckpoints, die Tumorzellen nutzen, um der Immunabwehr zu entkommen. Besonders bei PD-L1- positiven oder mikrosatelliteninstabilen (MSI) bzw. Tumoren mit der Defizienz der Mismatch-Reparatur (dMMR) wurde eine hohe Wirksamkeit beobachtet. Die aktuellen Indikationen mit Zulassung für die Immuncheckpoint-Inhibitoren im Bereich der gynäkologischen Onkologie sind in der Tabelle 2 zusammengefasst.
Tab. 2: In der Europäischen Union für die Behandlung von gynäkologischen Tumoren zugelassene Immuncheckpoint-Inhibitoren
Immuncheckpoint-Inhibitoren können eine Vielzahl sogenannter immunvermittelter Nebenwirkungen auslösen, die durch überschießende Aktivierung des Immunsystems entstehen. Am häufigsten betroffen sind Haut (Exanthem, Juckreiz), Gastrointestinaltrakt (Diarrhö, Kolitis), Leber (Hepatitis mit Transaminasenerhöhung), endokrine Organe (Hypo-/Hyperthyreose, Hypophysitis, Nebenniereninsuffizienz) sowie die Lunge (Pneumonitis). Leichtere Verläufe (Grad 1) können oft symptomatisch behandelt werden und erlauben eine Fortführung der Therapie unter Beobachtung. Bei moderaten bis schweren Toxizitäten (Grad ≥2) sind in der Regel eine Therapieunterbrechung und die Gabe von systemischen Kortikosteroiden (z.B. Prednisolon 0,5–2mg/kg) erforderlich; in therapierefraktären Fällen werden weitere Immunsuppressiva (z.B. Infliximab bei Kolitis) eingesetzt. Eine interdisziplinäre Betreuung (z.B. mit Endokrinologie, Gastroenterologie, Pneumologie) ist essenziell, um Komplikationen früh zu erkennen und die Sicherheit einer Fortführung der Immuntherapie zu gewährleisten.
Antikörper-Wirkstoff-Konjugate (ADC)
Eine sehr dynamische Entwicklung zeigt sich im Bereich der Antikörper-Wirkstoff-Konjugate (Antibody Drug Conjugate, ADC). ADC bestehen aus zwei Hauptkomponenten: einem monoklonalen Antikörper und einem potenten zytotoxischen Wirkstoff, der an den Antikörper gekoppelt ist. Diese Kombination ermöglicht es, den zytotoxischen Wirkstoff gezielt in die Tumorzellen zu bringen, die das entsprechende Antigen exprimieren.
Mit der 2024 erfolgten Zulassung von Mirvetuximab Soravtansin gibt es eine neue zielgerichtete Therapie zur Behandlung von Patient:innen mit fortgeschrittenem platinresistentem Ovarialkarzinom, deren Tumoren eine Überexpression des Folatrezeptor-alpha aufweisen. Mirvetuximab Soravtansin ist die erste Substanz, die im platinresistenten Setting einen Vorteil im Gesamtüberleben erreichen konnte. Im März wurde Tisotumab Vedotin – ein ADC gegen „tissue factor“ – in der EU für die Behandlung von Patient:innen mit rezidivierendem oder metastasierendem Zervixkarzinom zugelassen, das während oder nach einer Chemotherapie fortschreitet. Ein weiteres ADC, das an Bedeutung in der Therapie von gynäkologischen Malignomen zunimmt, ist Trastuzumab Deruxtecan. Diese Substanz zielt auf den humanen epidermalen Wachstumsfaktor-Rezeptor2 (HER2) ab. Auf der Grundlage einer tumoragnostischen Phase-II-Studie DESTINY-PanTumor02 erteilte die FDA dem Medikament kürzlich eine beschleunigte Zulassung für alle soliden Tumoren mit hoher HER2-Expression, die unter Standardtherapien progredient sind. Die Anwendung in der EU erfolgt derzeit „off-label“.
Die Toxizität der ADC ist substanzspezifisch. Die häufigsten Nebenwirkungen von Mirvetuximab Soravtansin sind ophthalmologische (verschwommenes Sehen, Keratopathie) und gastrointestinale Symptome wie Übelkeit, Erbrechen und Diarrhö. Für die Prävention der okulären Nebenwirkungen sind die Anwendung von benetzenden Augentropfen und augenärztliche Untersuchungen bei Beschwerden essenziell. Die bereits eingetretenen Nebenwirkungen können mit Therapiepausen und Dosisreduktion in den meisten Fällen behoben werden. In bestimmten Fällen müssen steroidhaltige Augentropfen angewendet werden. Auch bei Tisotumab Vedotin sind okuläre Toxizitäten typisch, hier werden sogar eine präventive Anwendung von steroidhaltigen Augentropfen sowie Augenkühlung während der Therapie empfohlen. Zudem werden periphere Neuropathien, Fatigue sowie hämatologische Nebenwirkungen beschrieben, die jedoch ebenfalls mit Therapiepausen, Dosisanpassungen und supportiven Maßnahmen erfolgreich behandelt werden können. Bei Trastuzumab Deruxtecan steht vor allem die interstitielle Lungenerkrankung (ILD) im Vordergrund. Daher sind frühes Erkennen (Bildgebung bei Symptomen wie Husten, Dyspnoe) und sofortige Unterbrechung der Therapie entscheidend. Bei bestätigter ILD sind die sofortige Therapieunterbrechung und die Einleitung einer Steroidtherapie erforderlich.
Literatur:
bei der Verfasserin
Das könnte Sie auch interessieren:
Neue Möglichkeiten der Gebärmuttertamponade bei postpartaler Hämorrhagie
Die postpartale Hämorrhagie (PPH) stellt weltweit eine der häufigsten Ursachen für maternale Mortalität dar. Schätzungen zufolge sterben global jährlich rund 70.000 Mütter an den Folgen ...
Mental health in the peri- and postmenopause
Menopause is a natural event, which is defined by the final menstrual period and is preceded by many years of “menopausal transition” associated with marked hormonal changes. Although ...
Das Bulboklitoralorgan in der gynäkologischen Praxis
Wohl kein anderes menschliches Organsystem kann auf eine ebenso spannende wie auch verstörende Geschichte zurückblicken wie die Vulva mit ihrer Hauptakteurin, dem Bulboklitoralorgan, das ...