Diagnostik, Überwachung und Therapie bei Präeklampsie
Autorin:
Dr. med. Lisa Lorenz-Meyer
Klinik für Geburtsmedizin
Campus Mitte
Charité – Universitätsmedizin Berlin
E-Mail: lisa.lorenz-meyer@charite.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Präeklampsie (PE) ist mit einem hohen Risiko für maternale und fetale Komplikationen verbunden und erhöht zugleich das langfristige kardiovaskuläre Risiko betroffener Frauen. Eine frühzeitige Diagnostik und Prophylaxe, eine rechtzeitige Entbindung sowie eine interdisziplinäre Nachsorge sind entscheidend für die Gesundheit von Mutter und Kind.
Hintergrund
Seit der Erweiterung der Definition im deutschsprachigen Raum 2019 wird die Präeklampsie als Hypertonie in Kombination mit einer typischen Organmanifestation definiert, auch ohne obligate Proteinurie ≥300mg/d. Diese Anpassung reflektiert die zugrunde liegende Pathophysiologie einer plazentaren Dysfunktion mit angiogener Dysbalance und generalisiertem Endothelschaden.1–3
Die Prävalenz stieg dadurch von 2,8% auf 3,4%, wobei die zusätzlich erfassten Patientinnen meist mildere Verläufe und seltener SGA-Neugeborene aufweisen.4 Weltweit sind hypertensive Schwangerschaftserkrankungen für etwa 16% der maternalen Todesfälle verantwortlich; das zwei- bis dreifach erhöhte kardiovaskuläre Langzeitrisiko ist hierin noch nicht berücksichtigt.5,6
Die Identifikation von Risikopatientinnen basiert auf einem Ersttrimesterscreening mit ggf. anschliessender ASS-Prophylaxe sowie der regulären Schwangerenvorsorge mit Blutdruck- und Urinkontrollen. Zur weiteren Risikoabschätzung eignet sich zwischen 19+0 und 24+6 SSW die Doppleruntersuchung der Aa. uterinae. Bei bestehenden Symptomen ab 24+0 SSW ist die Bestimmung des sFlt-1/PlGF-Quotienten sinnvoll, der sich insbesondere durch einen hohen negativen prädiktiven Wert (NPV) auszeichnet.7
Ersttrimesterscreening
In 11+0–13+6 SSW sollen alle Frauen über ein Präeklampsie-Screening informiert und der Algorithmus der Fetal Medicine Foundation angewandt werden, der die kombinierte Erhebung von A-priori-Risikofaktoren, der Blutdruckmessung und der Dopplermessung der Aa. uterinae und die Bestimmung der PlGF-Konzentration (falls PAPP-A bereits für das Aneuploidie-Screening der Biochemie bestimmt wurde, kann dies miteinbezogen werden) beinhaltet.7–9
Bei einem Risiko von >1:100 wird die abendliche Gabe von 150mg Acetylsalicyclsäure (ASS) bis zur 36. Schwangerschaftswoche empfohlen, wodurch das Auftreten einer PE ≤34 SSW um 62% gesenkt werden kann.10–12 Für Frauen mit Antiphospholipidsyndrom, Adipositas mit einem Body-Mass-Index ≥35, Diabetes und Nephropathie sowie vorbestehender Niereninsuffizienz sollte auch ohne vorheriges Präeklampsiescreening die Gabe von ASS erfolgen. Mendoza et al. weisen darauf hin, dass eine vorzeitige Beendigung zwischen 24 und 28 SSW bei im Verlauf unauffälligem Risikoprofil und normalem sFlt-1/PlGF-Quotienten erfolgen kann.13,14
Schwangerenvorsorge bei erhöhtem Risiko
Die Blutdruckmessung soll standardisiert im Sitzen nach einer fünfminütigen Ruhephase und an beiden Armen mit einer passenden Manschette erfolgen. Bei bekannter Hypertonie empfiehlt sich eine Heimblutdruckmessung an zwei bis drei Tagen wöchentlich, mindestens morgens.7 Der Zielblutdruckwert in der Schwangerschaft wurde auf ≤135/85mmHg gesenkt, da die strengere Einstellung in den CHIPS- und CHAP-Studien zu weniger kardiovaskulären Komplikationen bei unveränderter SGA-Rate führte.15,16
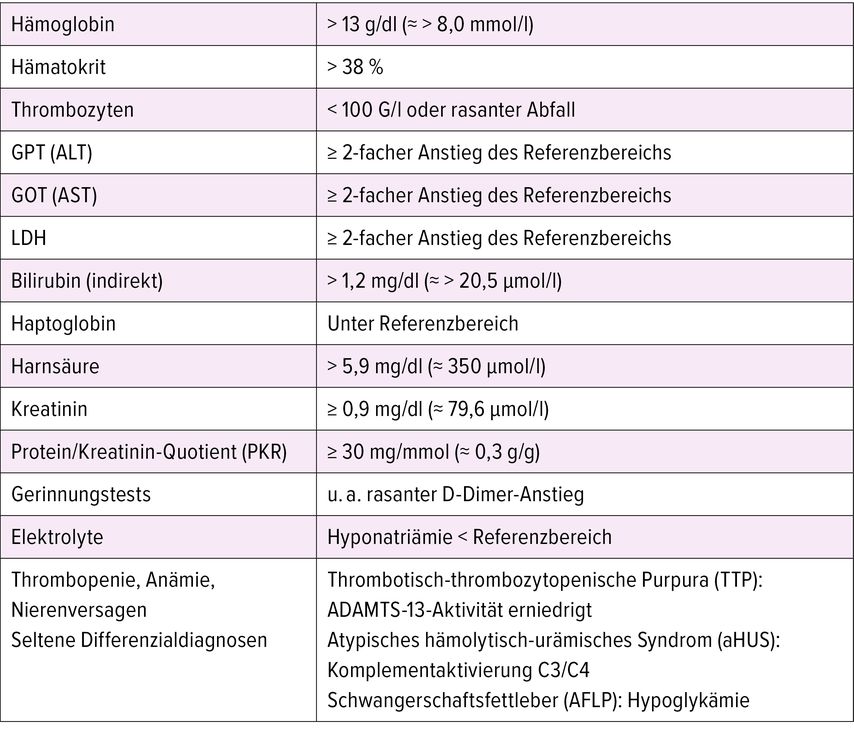
Bei ≥1 Proteinurie + im Urinstix soll der Protein-Kreatinin-Quotient bestimmt werden; ein Wert ≥30mg/mmol (300mg/g) gilt als auffällig und eine 24-h-Sammelurinbestimmung ist nicht nötig. Bei Verdacht auf Präeklampsie – insbesondere bei Symptomen wie Oberbauch- oder retrosternalen Schmerzen – sollten typische Laborveränderungen und ein HELLP-Syndrom (Hämolyse, erhöhte Leberwerte, Thrombopenie) abgeklärt werden, die Parameter sind in Tabelle 1 aufgeführt.
Ein niedriger sFlt-1/PlGF-Quotient <38 kann die Entwicklung einer Präeklampsie für bis zu vier Wochen ausschliessen, ein erhöhter sFlt-1/PlGF-Quotient >85 vor und >110 nach 34 Schwangerschaftswochen macht die Diagnose der Präeklampsie und präeklampsiebedingter Komplikationen wahrscheinlich.17–19 Abbildung 1 zeigt einen entsprechenden Handlungsalgorithmus.
Abb. 1: Handlungsalgorithmus nach sFlt-1/PlGF-Quotienten. Ein Cut-off-Wert zum Ausschluss der PE («Rule-out») gilt für alle Gestationsalter ab 24 Schwangerschaftswochen, die Diagnose der Präeklampsie («Rule-in») kann ≤34 SSW mit einem Cut-off-Wert >85 und >34 SSW mit einem Cut-off-Wert von 110 gestellt werden (modifiziert nach Verlohren et al., Cerdeira et al. und Zeisler et al.)17–21
Ambulantes Management
Eine ambulante Betreuung ist bei isolierter Hypertonie oder fetaler Wachstumsrestriktion möglich; bei manifester Präeklampsie oder Symptomverschlechterung ist jedoch eine umgehende Klinikvorstellung nötig.7 Ein sFlt-1/PlGF-Quotient 38 schliesst das Auftreten einer Präeklampsie mit hoher Sicherheit aus.20,21
Für die Langzeittherapie der Hypertonie stehen α-Methyldopa, Labetalol (in Österreich und der Schweiz), retardiertes Nifedipin sowie Metoprolol zur Verfügung. Die ISSHP empfiehlt die frühzeitige Kombinationstherapie, wenn der Blutdruck unter einer mittleren Dosierung eines Präparates nicht ausreichend kontrolliert werden kann.22
Hämodynamisch individualisierte Therapiekonzepte nach sogenannten Phänotypen der Präeklampsie mit hohem Gefässwiderstand und niedrigem Herzzeitvolumen vs. niedrigen Gefässwiderstand und hohes Herzzeitvolumen werden diskutiert, sind jedoch nicht evidenzbasiert.23,24 Daher sollte vorgeburtlich eine partizipative Entscheidung unter Berücksichtigung möglicher Nebenwirkungen erfolgen. Die Gabe von Pentaerythrityltetranitrat (PETN) zeigte in Studien bei pathologischer uteriner Durchblutung ein reduziertes Auftreten schwerer Hypertonien, ist jedoch für diese Indikation derzeit nicht zugelassen.25
Klinisches Management und Entbindung
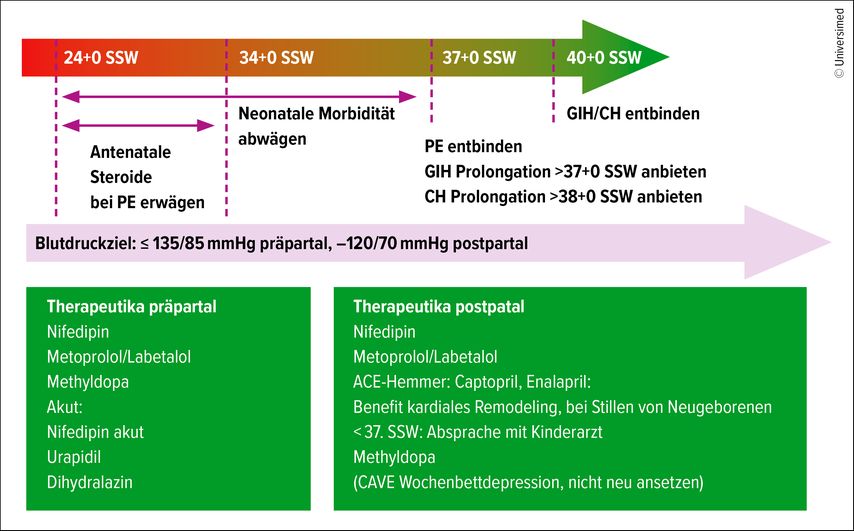
Das klinische Management bei Präeklampsie richtet sich nach dem Gestationsalter und ist in Abbildung 2 beschrieben.
Abb. 2: Vorgehen bei Präeklampsie in Abhängigkeit vom Gestationsalter und antihypertensive Therapeutika (modifiziert nach AWMF-Leitlinie)7
Wird eine manifeste Präeklampsie diagnostiziert, soll umgehend eine Klinikeinweisung erfolgen. Bei schweren neurologischen Symptomen, anhaltend hohen Blutdruckwerten ≥160/110mmHg bis hin zur hypertensiven Krise oder bei vitaler Bedrohung soll der Transport über das Rettungswesen erfolgen.7
Zur akuten Hypertoniebehandlung eignen sich kurz wirksames Nifedipin per os, intravenöses Urapidil oder Labetalol und in zweiter Linie auch Dihydralazin. Bei schwerer Hypertonie oder neurologischen Symptomen wie Sehstörungen, gesteigerten Reflexen oder Kopfschmerzen soll Magnesiumsulfat intravenös prophylaktisch verabreicht werden. Einen experimentellen Ansatz der Behandlung der Präeklampsie in Einzelfalluntersuchungen stellt die extrakorporale Filtration des antiangiogen wirkenden Proteins sFlt-1 dar, medikamentöse Ansätze zur Inhibierung des sFlt-1 werden untersucht, stehen aber noch nicht zur Verfügung.26
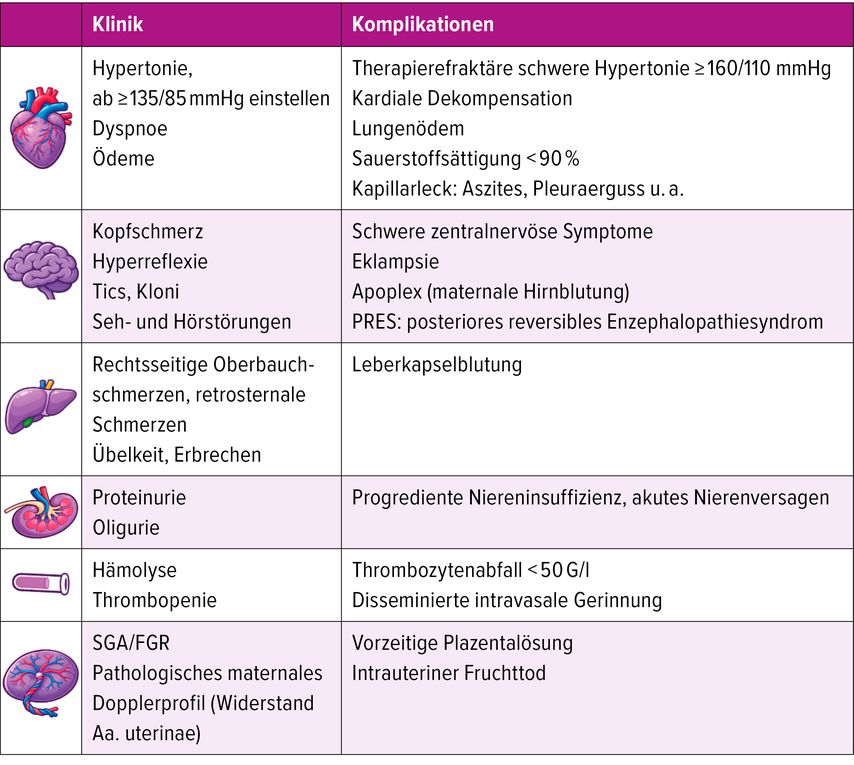
Bei schweren für Mutter oder Kind vital bedrohlichen Symptomen (Tab. 2) muss die Entbindungsindikation rechtzeitig gestellt werden. 2024 einigten sich Experten nach einem «Delphi Consensus Procedure» auf absolute Entbindungsindikationen bei früher Präeklampsie, deren Wertigkeit wird aktuell in der prospektiven AsSeDePre-32-Studie untersucht.27
Tab. 2: Klinische Zeichen und schwere Komplikationen bei Präeklampsie (modifiziert nach AWMF-Leitlinie)7
Neben dem Vorhandensein von Symptomen entscheidet das Gestationsalter über notwendige Massnahmen bei Präeklampsie. Vor 34+0 SSW muss die drohende kindliche und maternale Morbidität berücksichtigt werden und auch die Gabe einer antenatalen Steroidprophylaxe erwogen werden. Obwohl die Einbeziehung des sFlt-1/PlGF-Quotienten hierzu nicht in den nationalen Leitlinien empfohlen ist, ist ein klarer Zusammenhang zwischen kurzer verbleibender Schwangerschaftsdauer und erhöhtem sFlt-1/PlGF-Quotienten nachgewiesen worden.19, 28 In der Konsequenz sollte bei frühen klinischen Zeichen und hohem sFlt-1/PlGF-Quotienten also eine engmaschige, gegebenenfalls stationäre Überwachung erfolgen und die antenatale Steroidprophylaxe thematisiert werden. Für eine Bestimmung von sFlt-1/PlGF-Cut-off-Werten für die indizierte Entbindung, ACS oder notwendige stationäre Betreuung ist die aktuelle Datenlage aber nicht ausreichend.29–31
Nach 37 Schwangerschaftswochen bietet die Prolongation bei manifester Präeklampsie keine Vorteile mehr und die Entbindung sollte per Einleitung oder Kaiserschnitt angestrebt werden.7 Im Gegensatz dazu ist eine Schwangerschaftsprolongation bei gut eingestellter chronischer Hypertonie (CH) oder Gestationshypertonie (GIH) neuerdings nach den 2024 publizieren Leitlinien auch bis zum errechneten Geburtstermin vertretbar.7
Postpartale Nachsorge
Mit dem zunehmenden Verständnis des Risikos für kardiovaskuläre Ereignisse nach Präeklampsie entwickeln sich interdisziplinäre Empfehlungen für ein strukturiertes Nachsorgekonzept. Im angloamerikanischen Raum entsteht parallel dazu die Nischendisziplin «cardio-obstetrics».32
Die Leitlinien empfehlen derzeit die Aushändigung eines Nachsorgepasses, der über Lebensstilmassnahmen informiert und internistische Kontrollen nach sechs Wochen, sechs Monaten und einem Jahr vorsieht. Dabei sollen Blutdruck, Nierenfunktions- und Fettstoffwechselparameter überprüft werden.7 Im Wochenbett steht vor allem die suffiziente Blutdrucktherapie mit einem Zielblutdruck für gesunde junge Frauen von 120/70mmHg im Vordergrund.33 Da α-Methyldopa mit einem Risiko für postpartale Depression assoziiert ist, sollte postpartal auf andere Antihypertensiva zurückgegriffen werden.7 Die positiven Effekte von ACE-Hemmern auf das kardiale Remodeling26 tragen hier dazu bei, dass zunehmend Enalapril und Captopril eingesetzt werden. Auch wenn die Übertrittsrate in die Muttermilch insgesamt als gering eingeschätzt wird, sind zukünftig aber noch Anwendungsstudien nötig, die die begrenzte Datenlage über die Wirkung von ACE-Hemmern auf das gestillte Neu- und Frühgeborene verbessern.34–36
Literatur:
1 Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF). Hypertensive Schwangerschaftserkrankungen: Diagnostik und Therapie (S2k, AWMF-RegistryNo: 015/018, März 2019) [Internet]. [zitiert 20.September 2022]. Verfügbar unter: https://register.awmf.org/assets/guidelines/015- 018l_S2k_Diagnostik_Therapie_hypertensiver_Schwangerschaftserkrankungen_2019-07.pdf 2 Brown MA et al.: Hypertensive disorders of pregnancy: ISSHP classification, diagnosis, and management recommendations for international practice. Hypertension 2018; 72(1): 24-43 3 Gestational Hypertension and Preeclampsia: ACOG Practice Bulletin, Number 222. Obstet Gynecol 2020; 135(6): e237-60 4 Khan N et al.: Impact of new definitions of pre-eclampsia on incidence and performance of first-trimester screening. Ultrasound Obstet Gynecol 2020; 55(1): 50-7 5 Turbeville HR, Sasser JM: Preeclampsia beyond pregnancy: long-term consequences for mother and child. Am J Physiol-Ren Physiol 2020; 318(6): F1315-26 6 Global and regional causes of maternal deaths 2009–20: a WHO systematic analysis - The Lancet Global Health [Internet]. [cited 2025 May 6]. Available from: https://www.thelancet.com/journals/langlo/article/PIIS2214-109X(24)00560-6/fulltext 7 Hypertensive Disorders in Pregnancy: Diagnosis and Therapy. Guideline of the German Society of Gynecology and Obstetrics (S2k-Level, AWMF Registry No. 015/018, June 2024). https://register.awmf.org/de/leitlinien/detail/015-018 8 Poon LC, Nicolaides KH: Early prediction of preeclampsia. Obstet Gynecol Int 2014; 2014: 297397 9 Benkő Z et al.: Prediction of pre-eclampsia in twin pregnancy by maternal factors and biomarkers at 11-13weeks’ gestation: data from EVENTS trial. Ultrasound Obstet Gynecol Off J Int Soc Ultrasound Obstet Gynecol 2021; 57(2): 257-65 10 Rolnik DL et al.: Aspirin versus placebo in pregnancies at high risk for preterm preeclampsia. N Engl J Med 2017; 377(7): 613-22 11 Tan MY et al.: Screening for pre-eclampsia by maternal factors and biomarkers at 11-13weeks’ gestation. Ultrasound Obstet Gynecol Off J Int Soc Ultrasound Obstet Gynecol 2018; 52(2): 186-95 12 Bujold E et al.: Prevention of preeclampsia and intrauterine growth restriction with aspirin started in early pregnancy: a meta-analysis. Obstet Gynecol 2010; 116(2 Pt 1): 402-14 13 Mendoza M et al.: Aspirin discontinuation at 24 to 28 weeks’ gestation in pregnancies at high risk of preterm preeclampsia: a randomized clinical trial. JAMA 2023; 329(7): 542 14 Bonacina E et al.: Mid-trimester uterine artery Doppler for aspirin discontinuation in pregnancies at high risk for preterm pre-eclampsia: Post-hoc analysis of STOPPRE trial. BJOG Int J Obstet Gynaecol 2024; 131(3): 334-42 15 Tita AT et al.: Treatment for mild chronic hypertension during pregnancy. N Engl J Med 2022; 386(19): 1781-92 16 Magee LA et al.: The CHIPS randomized controlled trial (control of hypertension in pregnancy study): Is severe hypertension just an elevated blood pressure? Hypertension 2016; 68(5): 1153-9 17 Verlohren S et al.: An automated method for the determination of the sFlt-1/PIGF ratio in the assessment of preeclampsia. Am J Obstet Gynecol 2010; 202(2): 161.e1-161.e11 18 Verlohren S et al.: New gestational phase-specific cutoff values for the use of the soluble fms-like tyrosine kinase-1/placental growth factor ratio as a diagnostic test for preeclampsia. Hypertension 2014; 63(2): 346-52 19 Dröge LA et al.: Prediction of preeclampsia-related adverse outcomes with the sFlt-1 (soluble fms-like tyrosine kinase 1)/PlGF (placental growth factor)-ratio in the clinical routine: a real-world study. Hypertension 2021; 77(2): 461-71 20 Cerdeira AS et al.: Randomized interventional study on prediction of preeclampsia/eclampsia in women with suspected preeclampsia: INSPIRE. Hypertension 2019; 74(4): 983-90 21 Zeisler H et al.: Predictive value of the sFlt-1:PlGF ratio in women with suspected preeclampsia. N Engl J Med 2016; 374(1): 13-22 22 Magee LA et al.: The 2021 International Society for the Study of Hypertension in Pregnancy classification, diagnosis & management recommendations for international practice. Pregnancy Hypertens 2022; 27: 148-69 23 Valensise H et al.: Early and late preeclampsia: two different maternal hemodynamic states in the latent phase of the disease. Hypertension 2008; 52(5): 873-80 24 Masini G et al.: Preeclampsia has two phenotypes which require different treatment strategies. Am J Obstet Gynecol 2022; 226(2): S1006-18 25 Groten T et al.: The nitric oxide donor pentaerythritol tetranitrate lowers hypertension and angiogenic imbalance in pregnancies with impaired uterine perfusion—a secondary analysis of a randomized trial. Am J Obstet Gynecol 2025; S0002-937825007343 26 Thadhani R et al.: Pilot study of extracorporeal removal of soluble Fms-Like tyrosine kinase 1 in preeclampsia. Circulation 2011; 124(8): 940-50 27 Brodowski L et al.: Assessing severity and need for delivery in early onset preeclampsia before 32 weeks of gestation: a Delphi Consensus Procedure. Geburtshilfe Frauenheilkd 2024; 84(8): 760-72 28 Rana S et al.: Angiogenic factors and the risk of adverse outcomes in women with suspected preeclampsia. Circulation 2012; 125(7): 911-9 29 Enengl S et al.: Risk for imminent delivery in preeclampsia based on the sFlt-1/PlGF ratio: Do we need new cut-offs? Geburtshilfe Frauenheilkd 2025; 85(2): 190-9 30 Stolz M et al.: An sFlt-1:PlGF ratio of 655 is not a reliable cut-off value for predicting perinatal outcomes in women with preeclampsia. Pregnancy Hypertens 2018; 11: 54-60 31 Siepen C, Brennecke S: Does a sFlt-1/PlGF ratio result > 655 before 34 weeks’ gestation necessitate preterm delivery within 2 days? A retrospective observational study. J Matern Fetal Neonatal Med 2024; 37(1): 2371047 32 Sharma G et al.: Cardio-obstetrics. J Am Coll Cardiol 2020; 75(11): 1355-9 33 Arzneimittelkommission der Deutschen Apotheker (AMK), Arzneimittelkommission der Deutschen Ärzteschaft (AkdÄ), Deutsche Arbeitsgemeinschaft Selbsthilfegruppen E. V. (DAG SHG), Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin E. V. (DEGAM), Deutsche Gesellschaft Für Endokrinologie E. V. (DGE), Deutsche Gesellschaft Für Innere Medizin E. V. (DGIM) et al.: NVL Hypertonie – Langfassung [Internet]. Bundesärztekammer (BÄK); Kassenärztliche Bundesvereinigung (KBV); Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF); 2023 [cited 2025 Dec 17]. Available from: https://www.leitlinien.de/themen/hypertonie/pdf/hypertonie-vers1-0-lang.pdf 34 Ormesher L et al.: Postnatal enalapril to improve cardiovascular function following preterm preeclampsia (PICk-UP): a randomized double-blind placebo-controlled feasibility trial. Hypertension 2020; 76(6): 1828-37 35 Redman CWG et al.: The excretion of enalapril and enalaprilat in human breast milk. Eur J Clin Pharmacol 1990; 38(1): 99 36 Devlin RG, Fleiss PM: Captopril in human blood and breast milk. J Clin Pharmacol 1981; 21(2-3): 110-3
Das könnte Sie auch interessieren:
Schwangerenvorsorge in Deutschland
Die Schwangerenvorsorge begleitet werdende Mütter vom Beginn der Schwangerschaft bis zur Geburt. Sie dient der frühzeitigen Erkennung von Risiken, der Überwachung der kindlichen ...
Diagnostik und Therapie des Zervixkarzinoms
Weltweit werden jährlich über 500000 neue Zervixkarzinome diagnostiziert, überwiegend in ressourcenarmen Regionen. Dagegen sind Zervixkarzinome in entwickelten Ländern extrem selten ...
Breast reconstruction in obese patients: challenges and strategies
Obesity has emerged as one of the most prevalent chronic diseases in Europe and represents a major challenge for contemporary surgical care. Defined by the World Health Organization (WHO ...